این عنصر توسط Etal / A.Ghiorso و در سال 1969 در آمریکا کشف شد و به افتخار ارنست رادرفورد ( Ernest Rutherford ) نامگذاری شد .
این عنصر دارای سینتیک رادیواکتیو عنصری بالایی دارد و ایزوتوپ های پایداری را نیز دارد که نیمه عمر آن کمتر از 70 ثانیه است . این عنصر مشخصاتی مشابه عنصر هافنیم دارد . برای مثال به شکل یک ترکیب نسبتاً فرار با کلر است . گروهی از دانشمندان آزمایشاتی برای احراز هویت این عنصر انجام دادند و این کوشش های انجام گرفته نشان داد که در 3/0 ثانیه فعالیت در شکل فرار نشان داده است .
در مورد عناصر واسطه بايد گفت که رسانايي الکتريکي و قسمت اعظم خواص فلزي مربوط به درياي الکتروني الکترونهاي غيرمستقر سطح والانس است که مثلاً تعداد آنها در مورد منگنز، آهن و نيکل 2 است. الکترونهاي موجود در اوربيتالهاي اين عناصر نقش مستقيمي در پيوند فلزي مورد بحث ما در اين مدل ساده ندارند ولي در مجموع روي استحکام پيوند فلزي اثر مهمي ميگذارند.
فلزات واسطه به کار رفته در مصالح ساختماني و ماشينآلات از قبيل کروم، منگنز و آهن آرايشهاي اوربيتالي زير را دارند:
اين اتمها داراي تعداد قابل توجهي اوربيتالهاي تک الکتروني بوده که در بلور فلزي، با اوربيتالهاي تکالکتروني مجاور، اندکي همپوشاني کرده و نوعي پيوند کوالانسيبوجود ميآورند که بر استحکام و سختي فلز ميافزايد و عامل مهمي در افزايش نقطه ذوب آن محسوب ميشود.
در آلياژها نيز معمولاً همين اوربيتالهاي تک الکتروني از اتم يک فلز با اوربيتالهاي تکالکتروني عنصر يا عناصر انتخابي ديگر همپوشاني کرده و آلياژهايي با خواص مختلف و مطلوب پديد ميآورند.
در این آموزش تعاملی، دانش آموزان دوره دبستان و راهنمایی با نماد علمی و شکل مولکول های برخی از مواد آشنا می شوند.
در محیط تعاملی زیر، ذره بین را روی ماده ای قرار دهید که نام آن نوشته شده است و سپس با توجه به ماده، روی اتم های مورد نیاز برای ایجاد ماده کلیک کنید.
تا وقتی که گزینه صحیح را انتخاب نکنید، ماده بعدی مشاهده نخواهد شد.
مـاده:
تمام موادي را كه جهان از آن تركيب يافته است بر روي هم ماده ميگوييم ماده را ميتوان به صورت چيزي تعريف كرد كه جرم دارد و فضا اشغال ميكند . جرم پيمانهاي از كميت ماده است جسمي كه تحت تأثير نيروي خارجي نيست مايل است كه به حال سكون بماند و اگر در حال حركت باشد مايل است كه به حركت يكنواخت خود در همان جهتي كه دارد ادامه دهد اين خاصيت (اينرسي ) ناميده ميشود.
وزن ماده:
جرم يك جسم تغيير ناپذير است اما وزن ن چنين نيست وزن نيروي جاذبه گرانشي است كه از طرف زمين بر جسم وارد ميشود بنابراين وزن يك جسم معين بر حسب فاصله آن از مركز زمين تغيير ميكند وزن جسم با جرم آن و با جاذبه گرانشي زمين نسبت مستقيم دارد.
بنابراين در هر جاي معين دو جسم كه جرم مساوي داشته باشند وزن آنها با هم برابر است.
عنصر:
يونانيان باستان به اين مفهوم رسيده بودند كه كل ماده از تعداد محدودي مواد ساده كه آنها را عنصر ميناميدند تركيب يافته است . يونانيان كل ماده موجود در زمين را مشتق از چهار عنصر ؛ خاك ، هوا ، آتش و آب ميدانستند . از آنجا كه اجرام آسماني كامل و تغيير ناپذير دانسته ميشد آنان جرم فلكي را مركب از عنصر پنجمي به نام اتر در نظر ميگرفتند. اتر بعداً به نام quinessence از واژه لاتين به معني عنصر پنجم معروف شد.
اين نظريه يوناني قرنها تسلط خود را بر انديشههاي علمي حفظ كرد. در سال 1661 رابرت بويل در كتاب خود به اين عنوان شيميدان شكاك تعريف كاملاً جديد براي عنصر ارائه كرد : « اكنون منظور من از عناصر اجسام اوليه و ساده يا كاملاً غير آميختهاي كه از هيچ گونه اجسام يا از يكديگر ساخته نشده باشد آنها اجزاي اجسامي هستند كه وقتي كاملاً با هم آميخته شوند فوراً با هم تركيب ميشوند و آن اجسام در نهايت به اين اجزا تجزيه ميشوند.
بويل براي مشخص كردن اين مواد خامي كه عنصر ميناميدند اقدامي نكرد اما او تأكيد كرد كه دليل وجود اين عناصر همچنين تشخيص آنها موكول به آزمايش شيميايي است مفهومي كه بويل از عناصر شيميايي بدست اورده بود در سده بعد بوسيله آنتوان لاوازيه به نحوي پا برجا استقرار يافت لاوازيه مادهاي را به عنوان عنصر پذيرفت كه به مواد سادهتري تجزيه نشود علاوه بر اين او نشان داد كه يك ماده مركب از اتحاد عناصر توليد ميشود لاوازيه 23 عنصر را به درستي مشخص كرد گرچه او نور ، گرما و چند ماده مركب ساده را پيوست فهرست خود كرده بود.
هر عنصري بنا بر موافقت بين المللي با يك نماد شيميايي نشان داده ميشود غالب اين نهادها مركب از يك يا دو حرف است نهادهاي سه حرفي براي غالب عناصري كه اخيراً كشف و از طريق واكنشهاي هستهاي تهيه شدهاند بكار برده ميشوند.
مواد مركب:
مواد مركب موادي هستند كه از دو يا چند عنصر به نسبت ثابت تركيب يافتهاند قانون نسبتهاي مشخص كه نخستين بار در 1799 بوسيله ژورف پروست پيشنهاد شد ميگويد كه يك ماده مركب خالص همواره از عناصر يكسان و با نسبت جرمي يكسان تركيب يافتهاند مثلاً آب هميشه از عناصر هيدروژن و اكسيژن به نسبت 19% و 11% هيدروژن و % 81 و 88 اكسيژن توليد ميشود. بيش از دوازده هزار ماده مركب معدني شناخته شده است و بيش از چهار ميليون ماده سنتز شده يا از منابع طبيعي بدست آمدهاند خواص ماده مركب با خواص عناصر تشكيل دهنده اين مواد كاملاً متفاوت است.
ماده خالص و مخلوط :
يك عنصر يا يك ماده مركب را ماده خالص ميگويند تمام انواع ديگر ماده مخلوط هستند. مخلوطها از دو يا چند ماده خالص توليد ميشوند و تركيب درصدهاي قابل تغيير دارند خواص يك مخلوط بستگي به تركيب درصد مخلوط و خواص يك مخلوط بستگي به تركيب درصد مخلوط و خواص مواد خالصي دارد كه آن مخلوط را بوجود آوردهاند.
دو نوع مخلوط وجود دارد « مخلوط ناهمگن » و « مخلوط همگن »:
مخلوط ناهمگن كاملاً يكنواخت نيست بلكه مركب از اجزايي است كه از لحاظ فيزيكي متمايز از يكديگرند . مخلوط همگن كاملاً يكنواخت به نظر ميرسد و آن را محلول ميگويند . هوا ، نمك حل شده در آب و آلياژ نقره طلا ، به ترتيب نمونههايي از يك محلول گازي يك محلول مايع و يك محلول جامد است.
فـاز
بخشي از ماده را كه از لحاظ فيزيكي مشخص و تركيب درصد و خواص آن تماماً يكنواخت باشد فاز ميگويند . مواد همگن تنها مركب از يك فاز هستند و مواد ناهمگن بيش از يك فاز دارند فازهاي مخلوطهاي ناهمگن حدود مشخص دارند و معمولاً به آساني قابل تميزند . مثلاً در گرانيت كه يك مخلوط ناهمگن است بلورهاي صورتي و رنگ فلوسپار ، بلورهاي كوارتز بيرنگ و بلورهاي سياه و درخشان ميكا قابل تشخيص است.
وقتي تعداد فازهاي يك نمونه معين شود تمام بخشهايي از آن كه از يك نوعاند تنها يك فاز به حساب ميآيند . بنابراين گرانيت مركب از سه فاز است البته اجزاي نسبي سه فاز گرانيت ممكن است از نمونهاي به نمونه ديگر تفاوت داشته باشند.
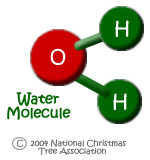
مولکول ها چیز خاصی نیستند. یک سری ذرات ریزه میزه هستند که با تجمع خود مواد را تشکیل می دهند. مثلا یک مشت آب از روی هم جمع شدن تعداد بسیار بسیار زیادی مولکول آب به وجود می آید. یک مولکول آب خودش از یک سری چیزهای های دیگر به اسم اتم به وجود می آید. اتم ها به تنهایی خاصیت خاصی ندارند. اما اگر چند اتم کنار هم قرار بگیرند مولکول به وجود می آید و مجموعه این چند اتم که مولکول نامیده می شوند، یکهویی صاحب خاصیت می شود. برای همین می گویند که مواد از مولکول ها ساخته می شوند. مولکول کوچکترین قسمت یک ماده است که خاصیت آن ماده را دارد.
مثلا یک اتم هیدروژن خاصیت خاصی ندارد.اما اگر یک اتم هیدروژن کنار یک اتم هیدروژن دیگر قرار بگیرد، یک مولکول گازی به وجود می آورد: یعنی گاز هیدروژن. یک اتم اکسیژن هم خاصیت خاصی ندارد اما اگر کنار یک اتم اکسیژن دیگر قرار بگیرد یک مولکول گازی مفید و حیاتی برای ما به وجود می آورند: گاز اکسیژن. اگر سه تا اتم اکسیژن کنار هم قرار بگیرند شکل دیگری از گاز را به وجود می آورند. گازی که لایه ازون را می سازد. بنابراین شکل کنار هم قرار گرفتن اتم ها، به اصطلاح پیوند بین اتم ها، مولکول های مختلف و در نتیجه مواد مختلف را به وجود می آورد.
کیک از آرد و تخم مرغ و شکر و یک سری چیزهای دیگر درست شده است. اما وقتی شما اول آرد بخورید، بعد شکر و بعد تخم مرغ، احساس می کنید کیک خورده اید؟ در واقع فکر کنم بیشتر احساس دل پیچه پیدا کنید!  به همین ترتیب با خوردن گاز هیدروژن و بعد گاز اکسیژن این احساس را ندارید که آب نوشیده اید. اول باید دوتا هیدروژن با یک اکسیژن به هم متصل شوند و بعد حالا اگر شما این ترکیب را بنوشید، تشنگی شما برطرف می شود.گرچه یک مولکول آب آنقدر ریزه میزه است که تشنگی شما برطرف نمی شود!!
به همین ترتیب با خوردن گاز هیدروژن و بعد گاز اکسیژن این احساس را ندارید که آب نوشیده اید. اول باید دوتا هیدروژن با یک اکسیژن به هم متصل شوند و بعد حالا اگر شما این ترکیب را بنوشید، تشنگی شما برطرف می شود.گرچه یک مولکول آب آنقدر ریزه میزه است که تشنگی شما برطرف نمی شود!! 
اتم ها مثل حروف الفبا می مانند. حروف الفبا به تنهایی معنای خاصی ندارند. مثلا حرف ک معنی خاصی ندارد. حرف ی هم معنی خاصی ندارد. حالا اگر من این حرف ها را با هم ترکیب کنم می شود کلمه کک که یک حشره خیلی ریزه پیزه سیاه کوچک است که آدم را می گزد. می شود از ترکیب این دو حرف کیک هم به دست آورد که خیلی هم خوشمزه و با مزه و شیرین است. مولکول ها مانند کلمات هستند. همانطور که حروف به هم متصل می شوند و کلمه می سازند، اتم ها هم به هم وصل می شوند تا مولکول ها را به وجود بیاورند.

اما چی باعث می شود که مولکول های یک ماده در کنار هم باقی بمانند؟
مولکول های مواد همدیگر را می ربایند. به همین علت مولکول های آب کنار هم باقی می مانند و از هم فاصله نمی گیرند. البته مقدار این ربایش در مواد جامد و مایع و گاز با هم فرق دارد. نیروی ربایش بین مولکول های گاز خیلی کم و تقریبا ناچیز است. برای همین مولکول های گاز تا جایی که بتوانند از هم دور می شوند و آزاد و رها هستند و برای خودشان تنهایی تاتی تاتی می کنند. به همین دلیل هواپیما راحت از توی هوا رد می شود! تصور کنید اگر ربایش بین مولکول های هوا زیاد بود برای هواپیما چه اتفاقی می افتاد؟!!

ربایش بین مولکول های جامد آنقدر زیاد است که به همین راحتی ها دست از سر هم بر نمی دارند و از کنار هم تکان نمی خورند. برای جدا کردن مولکول های جامد باید حسابی از زور بازو استفاده کنید. ( مثل خرد کردن قند یا شکستن چوب). برای همین تفاوت در مقدار ربایش، فاصله بین مولکول ها در سه حالت ماده با هم فرق دارد. خودتان می توانید حدس بزنید که در کدام حالت این فاصله بیشتر و در کدام حالت کمتر است.
نکته برای ششمی ها: پختن یک تغییر شیمیایی است. چون با پختن یک ماده غذایی شکل مولکول ها عوض می شود. مولکول های مختلف، مواد مختلف را به وجود می آورند. در واقع حرارت باعث می شود که شکل مولکول ها تغییر کند و اتم های جدیدی به دست بیاورند و یا حتی اتم هایی را از دست بدهند. مولکول نان، با مولکول آرد تفاوت دارد و تغییر شیمیایی یعنی تغییری که در آن ساختار ماده عوض شود و ماده تولید شده، با ماده قبلی فرق داشته باشد. اتفاقی که در پختن و در سوختن می افتد.
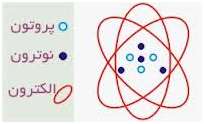
اَتُم (به انگلیسی: Atom) واژه ای است یونانی به معنی «ناگسستنی» (من تقسیم نمیشوم)[۲]، اتم واحد تشکیل دهنده تمام مواد (یا تک تک عناصر شیمیایی) است که متشکل از یک هسته مرکزی است که محاطه شده با ابر الکترونی با بار منفی. تعریف دیگری آن را به عنوان کوچکترین واحدی در نظر میگیرد که ماده را میتوان به آن تقسیم کرد بدون اینکه اجزاء بارداری از آن خارج شود.[۳] اتم ابری الکترونی، تشکیلشده از الکترونها با بار الکتریکی منفی، که هستهٔ اتم را احاطه کردهاست. هسته نیز خود از پروتون که دارای بار مثبت است و نوترون که از لحاظ الکتریکی خنثی است تشکیل شدهاست. زمانی که تعداد پروتونها و الکترونهای اتم با هم برابر هستند اتم از نظر الکتریکی در حالت خنثی یا متعادل قرار دارد در غیر این صورت آن را یون مینامند که میتواند دارای بار الکتریکی مثبت یا منفی باشد. اتمها با توجه به تعداد پروتونها و نوترونهای آنها طبقهبندی میشوند. تعداد پروتونهای اتم مشخص کننده نوع عنصر شیمیایی و تعداد نوترونها مشخصکننده ایزوتوپ عنصر است.[۴]

الکترون نامتمرکز (به انگلیسی: Delocalized electron) به الکترونهایی در یک مولکول گفته میشود که متعلق به یک اتم یا پیوند خاص نمیباشند. این الکترونها را میتوان در سیستمهای مزدوج و مزویونیک دید و نقش مهمی در تئوری اوربیتال مولکولی دارند. الکترونهای پیوند سیگما نیز نامتمرکزند.
کوارک (به انگلیسی: Quark) یک ذره بنیادی و بخش اساسی سازندهی ماده است. کوارکها با هم ترکیب میشوند تا ذرات مرکبی به نام هادرون را بهوجود آورند، پروتون و نوترون از معروفترین آنها هستند. مثلاً پروتون از دو کوارک بالا (Up quark) و یک کوارک پایین (Down quark) تشکیل شده است، در حالی که دو کوارک پایین و یک کوارک بالا، نوترون را میسازند.
 کوارک
Quark |
|
 ساختار کوارکی پروتون |
|
| ترکیب: | ذره بنیادی |
|---|---|
| خانواده: | فرمیون |
| گروه: | کوارک |
| رده: | ۱٬۲٬۳ |
| برهمکنش: | نیروی ضعیف٬نیروی قوی٬نیروی جاذبه٬نیروی الکترومغناطیس |
| ذره بنیادی: | آنتیکوارک (q) |
| پاد ذره بنیادی: | پاد پروتون |
| استدلال: | ماری گلمان (1964) جورج زویگ (1964) |
| کشف شده: | آزمایشگاه ملی شتابدهنده اسلاک (~1968) |
| نماد: | q |
| تعداد انواع: | (u, d, c, s, t، و b) |
| بار الکتریکی: | +2⁄3 e, −1⁄3 e |
| بار رنگ: | بله |
| اسپین: | 1⁄2 |
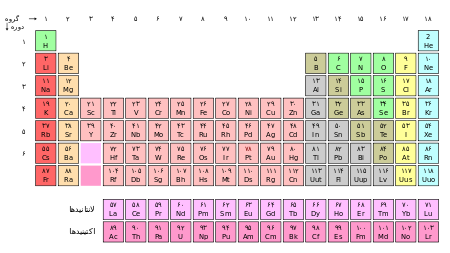
جدول تناوبی عنصرهای شیمیایی، نمایش جدولی عنصرهای شیمیایی بر پایهٔ عدد اتمی، آرایش الکترونی و ویژگیهای شیمیایی آنها است. ترتیب جایگیری عنصرها در این جدول از عدد اتمی کمتر به سوی عدد اتمی (شمار پروتونهای) بالاتر است. شکل استاندارد این جدول ۱۸ × ۷ است؛ عنصرهای اصلی در بالا و دو ردیف کوچکتر از عنصرها در پایین جای دارد. میتوان این جدول را به چهار مستطیل شکست، این چهار ستون مستطیلی عبارتند از: بلوک اس در سمت چپ، بلوک پی در راست، بلوک دی در وسط و بلوک اف یا همان فلزات واسطهٔ داخلی در پایین. ردیفهای این جدول، دوره و ستونهای آن یا همان ستونهای s و d و p، گروههای جدول تناوبی نام دارند. همچنین گاهی برخی از این گروههای نامهای ویژهای دارند برای نمونه گروه هالوژنها و گازهای نجیب از آن جملهاند. هدف از ساخت جدول تناوبی چه به شکل مستطیلی و چه به شکلهای دیگر برای بررسی بهتر ویژگیهای شیمیایی عنصرها بوده است این جدول کاربرد زیادی در دانش شیمی و پردازش رفتار عنصرها دارد.
 پروتون
|
|
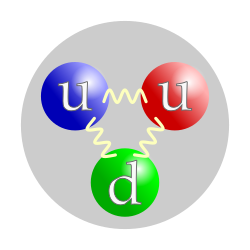 ساختار کوارکی پروتون |
|
| ترکیب: | ۲ بالا ۱ پایین |
|---|---|
| خانواده: | فرمیون |
| گروه: | کوارک |
| برهمکنش: | نیروی ضعیف٬نیروی قوی٬نیروی جاذبه٬نیروی الکترومغناطیس |
| پاد ذره بنیادی: | پاد پروتون |
| کشف شده: | ارنست رادرفورد (۱۹۱۹) |
| نماد: | p+ |
| جرم: | ۱٫۶۷۲ ۶۲۱ ۷1(29) × ۱۰−۲۷ kg ۱٫۰۰۷ ۲۷۶ ۴۶۶ ۸8(13) u |
| بار الکتریکی: | ۱٫۶۰۲ ۱۷۶ ۵3(14) × ۱۰−۱۹ C |
| اسپین: | ½ |
پروتون (Proton) ذرهای بنیادی با بار مثبت است که بخشی از هر اتم را تشکیل میدهد. جرم پروتون ۱۸۳۷ برابر جرم الکترون، و معادل ۱ amu است.
بر اساس قوانین پایستگی و به علت آنکه پروتون سبکترین باریون است پایدار است اما براساس نظریه وحدت بزرگ این ذره عمر ۱٫۶×۱۰۳۰ سال داشته و بعد از این مدت به پوزیترون و پیون صفر تبدیل میشود.[۱]
پروتون از دو کوارک بالا و یک کوارک پایین تشکیل شده است.[۲]
جستارهای وابسته
پانویس
- پرش به بالا ↑ Sarkar, Utpal. Particle and Astroparticle Physics. CRC Press, 2008. 213-214. ISBN ISBN 1-58488-931-4.
- پرش به بالا ↑ Encyclopedia of Nuclear Physics and its Applications, 390.
منابع
- Encyclopedia of Nuclear Physics and its Applications. 2012. Retrieved 2013-10-08.
- Proton definition
 نوترون
|
|
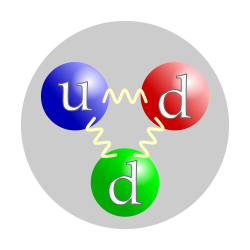 ساختار کوارکی نوترون |
|
| ترکیب: | ۲ پایین ۱ بالا |
|---|---|
| خانواده: | فرمیون |
| گروه: | کوارک |
| برهمکنش: | نیروی ضعیف٬نیروی قوی٬نیروی جاذبه٬نیروی الکترومغناطیس |
| پاد ذره بنیادی: | پاد نوترون |
| کشف شده: | جیمز چادویک[۱] |
| نماد: | n |
| جرم: | ۱٫۶۷۴ ۹۲۷ ۲۹(۲۸) × ۱۰−۲۷kg ۹۳۹٫۵۶۵ ۵۶۰(۸۱) الکترونولت/c² ۱٫۰۰۸۶۶۵ u |
| بار الکتریکی: | ۰ C |
| اسپین: | ½ |
نوترون یکی از ذرات هستهای اتم است. نوترون دارای بار الکتریکی خنثی است و به همراه پروتون در داخل هسته اتم اصل جرم اتم را تشکیل میدهند.
از هیدروژن (۱ پروتون) تا کلسیم (۲۰ پروتون) تعداد آن با تعداد پروتون یکی نیست و از آن بالاتر در جدول تناوبی تعدادش بیشتر میشود. جرم مطلق ۲۷- ۱۰ × ۱٬۶۷۴۸۲ کیلوگرم و جرم نسبی آن ۱٬۰۰۸۶۶۵۴۱ است. برای مثال ۵۶n بر روی Fe و p۲۶ بر زیر آن تشکیل دهندهٔ آهن است.
جیمز چادویک در سال ۱۹۳۲ نوترون را، که رادرفورد در سال ۱۹۲۰ وجود آن را پیشبینی کرده بود، کشف کرد. پروتونها ذراتی مثبت هستند و به شدت همدیگر را دفع میکنند علت اینکه پروتونها همدیگر را دفع نمیکنند نوترنها هستند. نوترون ذرهای ناپایدار است و عمر متوسط آن ۹۱۸ ثانیه است که به پروتون، الکترون و نوترینو واپاشیده میشود. به این واپاشی، واپاشی بتا میگویند اتمی که پرتوی بتا تابش میکند چون یک پروتون به پروتونهایش اضافه میشود به عنصر بالاتر سلف میکند در همه اتمها اینگونه نیست زیرا اصل طرد پائولی برای اتمهایی که نسبت نوترونهایش به پروتونهایش کمتر از ۱٫۵ است اجازه واپاشی نمیدهد.
نوترون از یک کوارک بالا و دو کوارک پایین ساخته شده است.[۲]
تاریخچه کشف نوترون
با اندازه گیریهایی که ارنست رادرفورد انجام داده بود، متوجه شد که جرم هسته اتم تقریبا دوبرابر تعداد پروتونها است. بدین ترتیب او پیش بینی کرد که ذرهای دیگر باید در هسته باشد تا این کمبود جرم را جبران کند.
در سال ۱۹۳۲ جیمز چادویک آزمایشی ترتیب داد. او بریلیم را با آلفا بمباران کرد و متوجه شد ذرهای با قدرت نفوذ بسیار بالا از هسته اتم بیرون میزند که در میدان مغناطیسی منحرف نمیشود. ابتدا فکر کرد باید اشعه X یا گاما باشد اما هنگامی که سرعت آن را اندازه گرفت متوجه شد سرعت این ذره یک دهم سرعت نور است. به همین دلیل این ذره را که جرم آن حدود جرم پروتون و بیشتر بود، بار الکتریکی نداشت و سرعت آن یک دهم سرعت نور بود نوترون نامید و آن را به هسته نسبت داد.
جستارهای وابسته
پانویس
منابع
Gregersen, E.. The Britannica Guide to Particle Physics. Britannica Educational Pub., 2011. Retrieved 2013-10-08
شیمی فراذرهای
شیمی فراذرهای یا شیمی مهمان-میزبان (به انگلیسی: Supramolecular chemistry) ، شاخهای از دانش شیمی است که به بررسی سیستمهای شیمیایی در تعداد زیادی از مولکولهای یک ماده و همچنین مطالعه نیروهای بین مولکولی می پردازد و در سال ۱۸۷۳ توسط یوهان دیدریک وان در والس پیشنهاد شد. این شاخه از دانش همچنین با نامهای شیمی سوپرامولکولی ، یا شیمی فرامولکولی نیز شناخته میگردد.
منبع
- ویکیپدیای انگلیسی
| این یک نوشتار خُرد پیرامون شیمی است. با گسترش آن به ویکیپدیا کمک کنید. |

ترموشیمی(به انگلیسی: Thermochemistry) علمی است که به مطالعه تغییرات گرما و انرژی در طی یک واکنش شیمیایی می پردازد.[۱]
منابع
- پرش به بالا ↑ Perrot, Pierre (1998). A to Z of Thermodynamics. Oxford University Press. ISBN 0-19-856552-6.
| این یک نوشتار خُرد پیرامون شیمی است. با گسترش آن به ویکیپدیا کمک کنید. |
بلورنگاری،بلورشناسی یا کریستالوگرافی (به انگلیسی: Crystallography) دانشی است که به قوانین حاکم بر حالت بلورین مواد جامد، آرایش اتمی/مولکولی بلورها، خواص فیزیکی و شیمیایی و ساخت، رشد و شناسایی بلورها میپردازد.
این علم در اول بدست زمینشناسان در شناسایی کانیها توسعه یافت سپس شیمیدانان این علم را برای شناسایی مواد بکار گرفتند. پس از آن فیزیکدانان با بکار گیری پراش اشعه ایکس به پیشبرد آن کمک کردند.
در بیشتر کشورها به ویژه در آلمان، بلورشناسی بخشی از کانیشناسی است ولی در کشورهایی مانند انگلستان و ایالات متحده غالبآ به صورت بخشی از فیزیک یا شیمی تدریس میشود.
اکثر کشورها یک کمیتهٔ ملی بلورشناسی دارند که نمایندهٔ اتحادیهٔ بینالمللی بلورشناسی است. این اتحادیه گاهنامهٔ آکتا کریستالوگرافیکا (یادداشتهای بلورشناختی) و جدولهای بینالمللی بلورشناسی را منتشر میکند.
داروشناسی یا فارماکولوژی (به انگلیسی: Pharmacology) شاخهای از پزشکی و زیستشناسی است که به مطالعه واکنش متقابل داروها (یا مواد شیمیایی) بر موجودات زنده٬ که منجر به ایجاد اثرات زیستشناسی این ترکیبات میگردد. داروشناسی شامل دو بخش فارماکودینامیک و فارماکوکینتیک است.[۱][۲]
ریشهٔ تاریخی فارماکولوژی بالینی به سدههای میانه و به کتاب پزشکی قانون نوشتهٔ ابن سینا و گزارشاسحاق نوشته پترس ایسپانوس و همچنین جانسنتآماند بازمیگردد.[۳]
سینتیک شیمیایی شاخهای از علم است که به مطالعهٔ سرعت فرآیندهای شیمیایی و عوامل موثر بر آنها میپردازد.
جستارهای وابسته
منابع
- مورتیمر، چارلز. «سینتیک شیمیایی». در شیمی عمومی. ترجمهٔ عیسی یاوری. ویرایش ویرایش ششم (۱۹۸۶). چاپ سی و یکم. تهران: نشر علوم دانشگاهی، ۱۳۸۸. ISBN 964-6186-33-5.
- James E.House, Principles of Chemical Kinetics, 2nd Ed., Elsevier Inc., United States of America, 2007. ISBN 978-0-12-356787-1
| این یک نوشتار خُرد پیرامون شیمی است. با گسترش آن به ویکیپدیا کمک کنید. |
معادله سرعت (به انگلیسی: Rate Equation) یا قانون سرعت معادلهای است که سرعت یک واکنش شیمیایی را به غلظت گونههای واکنشگر و پارامترهای مستقل از غلظت مانند درجهٔ جزئی واکنش و ضریب سرعت ارتباط میدهد. برای نمونه در واکنش A + B → C معادلهٔ سرعت بصورت زیر بیان میشود[۱]:
که در آن [X] غلظت واکنشگر X، k ثابت سرعت یا ضریب سرعت و m و n به ترتیب درجهٔ جزئی واکنش نسبت به واکنشگر A و B هستند.
منابع
- پرش به بالا ↑ James E.House, Principles of Chemical Kinetics, 2nd Ed., Elsevier Inc., United States of America, 2007. ISBN 978-0-12-356787-1
|
|||||||||||||||||
| این یک نوشتار خُرد پیرامون شیمی است. با گسترش آن به ویکیپدیا کمک کنید. |
سرعت واکنش (به انگلیسی: Reaction rate) مقدار پیشرفت واکنش بر حسب زمان است که معمولاً بصورت تغییرات غلظت یکی از گونههای درگیر واکنش بر حسب زمان بیان میشود. بنابراین دیمانسیون سرعت بایستی بر حسب غلظت بر زمان (مول/لیتر.ثانیه یا مول/لیتر.دقیقه و ...) باشد. سینتیک شیمیایی بخشی از علم شیمی است که سرعت واکنشها و عوامل موثر بر آن را بررسی میکند.[۱]
تعریف
به عنوان نمونه، در واکنش زیر:
- aA + bB → cC + dD
که در آن حروف کوچک (a، b، c و d) نشانگر ضرایب استوکیومتری و حروف بزرگ (A، B، C و D) نمایندهٔ واکنشگرها و محصولات هستند. سرعت واکنش (R) در سیستم بسته بصورت زیر بیان میشود[۲]:
منابع
- پرش به بالا ↑ James E.House, Principles of Chemical Kinetics, 2nd Ed., Elsevier Inc., United States of America, 2007. ISBN 978-0-12-356787-1
- پرش به بالا ↑ Ronald W. Missen, Charles A. Mims, Bradley A. Saville, Introduction to chemical reaction engineering and kinetics, John Wiley & Sons, United States of America, 1999. ISBN 0-471-16339-2
شیمی آب تجزیه و تحلیل و شناسایی آب و تعیین کمیت اجزای شیمیایی و خواص آب است که شامل آنیونها و کاتیونهای PH و عناصر کمیاب است. که در تحلیل شیمیآب بسیار مورد استفاده قرار میگیرد. تجزیه و تحلیل شیمی آب بیشتر در زمینه مطالعات کیفیت آب و آلودگی هوا و آبهای گرم زمین کاربرد دارد.
مواد و روشها
بسته به نوع اجزا روشهای مختلفی در تعیین مقدار و یا نسبت استفاده از اجزا وجود دارد. در حالی که برخی از روش ها را میتوان با تجهیزات آزمایشگاه انجام داد اما بعضی مواقع هم نیاز به دستگاههای پیشرفته، مانند القایی همراه پلاسما طیف سنجی جرمی (ICP-MS) است.
جستارهای وابسته
منابع
- مشارکتکنندگان ویکیپدیا، «Water chemistry analysis»، ویکیپدیای انگلیسی، دانشنامهٔ آزاد (بازیابی در ۲۹ مهر ۱۳۹۲).
شیمی بسپار یا پلیمر (به انگلیسی: Polymer Chemistry) و یا شیمی درشتمولکول (به انگلیسی: Macromolecular Chemistry) ، شاخهای از دانش شیمی است که در آن خواص شیمیایی و روش ساخت درشتمولکولها و بسپارها مورد مطالعه قرار میگیرد.
بسپارها، از بسپارش تکپارها تشکیل میشوند. در شیمیِ بسپار، درجه بسپارش ، توزیع جرمی مولی ، تاکتیسیته ، همپار و بسیاری موضوعات دیگر مورد بررسی هستند.
منابع
شیمی سنجی یا کمومتریکس (به انگلیسی: Chemometrics)، کاربرد علوم آمار، کامپیوتر، ریاضی و گرافیک برای در ک بهتر داده های شیمی میباشد. از روشهای ذکر شده برای درک بهتر اطلاعات شیمیایی که در آزمایشگاه بدست میآید استفاده میشود، به این صورت که با استفاده از آنالیز دادههای شیمیایی بدست آمده اطلاعات مفید استخراج میشود با توجه به این اطلاعات میتوان آزمایشهای مورد نظر با بازدهی بهتر را طراحی کرد. کاربرد روشهای ریاضی در شیمی سابقه دیرین دارد ولی با توجه به پیشرفت علوم کامپیوتر و کاربرد آن در علوم روشهای کمومتریکس در دهه اخیر پیشرفت بسیار داشتهاست. در این دو دهه روشهای کمومتریکس مختلفی توسط شیمیدانها با کمک متخصصین علوم کامپیوتر، ریاضی و آمار ارائه شدهاست. بسیاری از شیمیدانها، اسوانت وولد را به عنوان اولین کسی که این روشها را معرفی کردهاست نام میبرند و به او لقب پدر علم کمومتریکس را دادهاند. آقای H.wold در دهه ۶۰ میلادی مقالات بسیاری تحت عنوان معرفی روشهای ریاضی و کاربرد آنها در شیمی ارائه کردهاست. سابقه استفاده و مطالعه روشهای کمومتریکس در ایران حدود ۱۰ سال میباشد که در دانشگاههای مختلف این مطالعات انجام میشود.
پیشرفت کمومتریکس در ایران در دهه اخیر توسط بسیاری از محققین شیمی تجزیه در دانشگاه های مختلف رو به رشد می باشد. از دانشگاه های فعال در زمینه کمومتریکس در ایران می توان دانشگاه های خواجه نصیر الدین طوسی - دانشگاه رازی - تحصیلات تکمیلی زنجان - دانشگاه شیراز - دانشگاه آزاد اسلامی اراک را نام برد. همچنین هر ساله به همت دانشگاه تحصیلات تکمیلی زنجان و دکتر حمید عبدالهی کارگاه کمومتریکس در این دانشگاه برگزار می گردد. همچنین می توان از دکتر جهانبخش قاسمی - دکتر حمید عبدالهی - دکتر بهرام همتی نژاد - دکتر محسن کمپانی - دکتر علی نیازی - دکتر مرتضی بهرام - دکتر عبدالحسین ناصری بعنوان محققین فعال در این زمینه در ایران نام برد.
منابع
- ویکیپدیا انگلیسی


![R; =; k [ A ]^{m}[ B ]^{n}](http://upload.wikimedia.org/math/a/b/6/ab65a9179de26a83ea2a2e5ab508ab24.png)
![R = - frac{1}{a} frac{d[A]}{dt} = - frac{1}{b} frac{d[B]}{dt} = frac{1}{c} frac{d[C]}{dt} = frac{1}{d} frac{d[D]}{dt}](http://upload.wikimedia.org/math/9/0/6/9067c70249870709b1c247159f70ae50.png)

 رادرفوردیم
رادرفوردیم